줄기세포치료제, 바이오소재, 조직공학, 면역세포치료제, 유전자치료제 분야를 아우르는 재생의료가 난치성 질환의 치료 대안으로 부각되고 있는데요. 코로나19의 영향에도 불구하고 재생의료산업은 미국, 유럽 등 선진국을 중심으로 정부 및 민간 투자가 활발히 이루어지면서 큰 폭으로 성장하고 있습니다.
이번 포스팅에서는 한국바이오협회가 발행한 <글로벌 첨단바이오의약품 산업 동향> 보고서를 통해 재생의료산업의 동향과 전망에 대해 살펴보도록 하겠습니다.
재생의료란

재생의료란 ‘손상된 인체 세포와 조직, 장기를 대체하거나 재생함으로써 정상기능을 복원하거나 새로 만들어내는 의료기술’을 말하는데요. 인체의 세포와, 조직, 장기를 구조적으로 대체하거나 복원하는 것뿐만 아니라 기능적으로 대체하거나 복원하는 것도 포함하고 있으며, 이를 체외에서 제작하여 손상된 인체 부위를 대체하는 기술과 인체가 스스로 자가 재생하도록 촉진하는 기술을 모두 포함합니다. 초기에는 체세포 또는 줄기세포를 이용하여 새로운 치료용 세포와 조직을 제작하는 기술을 의미하였으나 현재는 다양한 약물, 소재 및 의료기기 등을 이용하여 손상된 인체 부위의 재생을 촉진하는 기술까지 포괄하는 개념으로 사용되고 있습니다.1)
재생의료산업 현황
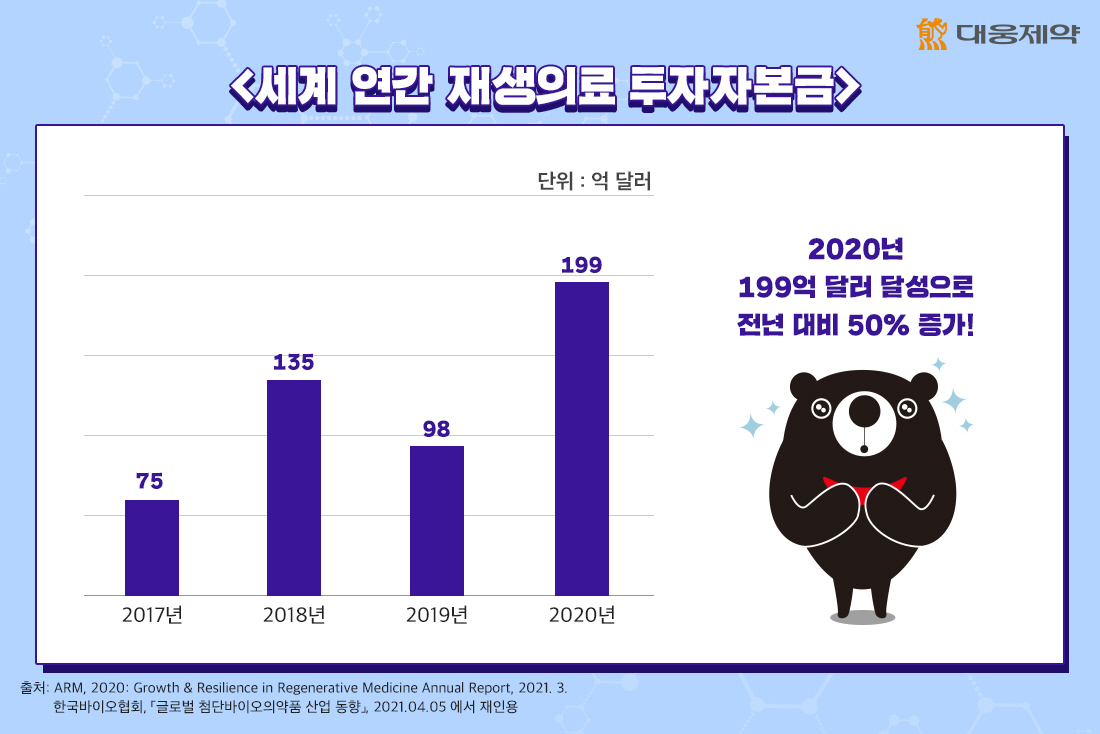
재생의료산업은 코로나19에도 불구하고 2020년 큰 폭으로 성장하였는데요. 2020년 세계 재생의료산업에는 전년 대비 50% 증가한 199억 달러(약 22조 3,297억 원)의 투자 자금이 조달되며 iPSC(유도만능줄기세포), 유전자 편집, 동종이계 세포 면역치료 등의 분야에서 성과를 보였습니다.
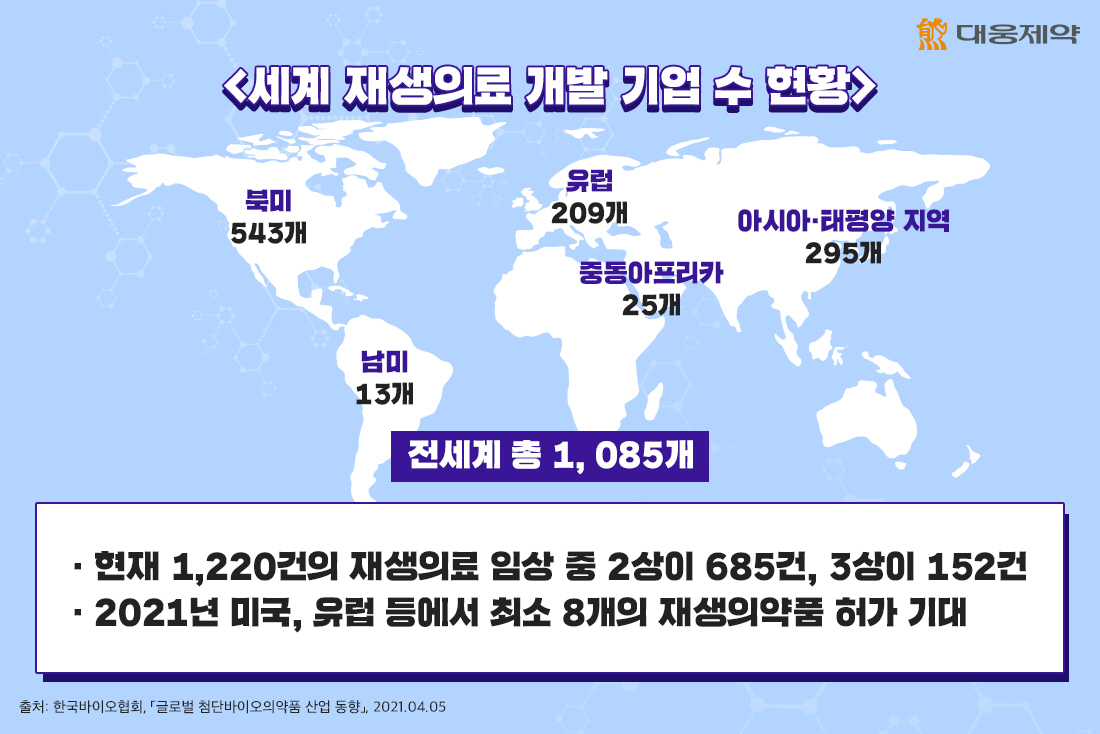
이러한 적극적인 투자의 결과로 전세계 유전체, 세포 및 조직 기반 치료제 개발 업체는 총 1,085개(2021년 3월 기준)에 달하는데요. 지역별로 살펴보면, 북미가 543개로 가장 많고, 그 뒤를 이어 아시아·태평양 지역이 295개, 유럽 209개, 중동아프리카와 남미가 각각 25개, 13개를 차지하고 있습니다.
이들 업체를 통해 현재 전세계적으로 총 1,220건의 재생의료 임상이 이루어지고 있는데요. 그 중 2상이 685건으로 가장 많고, 152건이 3상 진행중에 있어 2021년에는 미국, 유럽 등에서 최소 8개의 재생의약품 허가가 기대되고 있습니다.
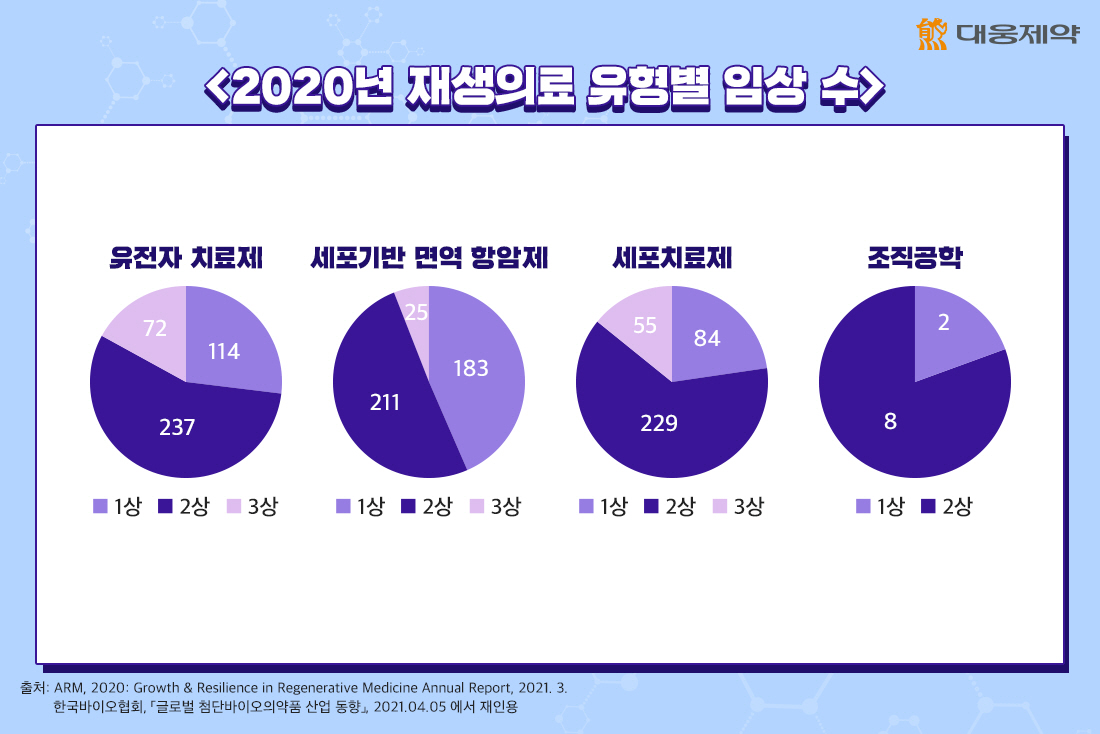
유형별로는 유전자치료제의 경우 임상 2상에 237건, 임상 3상에 72건이 진행되고 있는데요. 세포기반 면역항암제의 경우도 임상 2상에 211건, 임상 3상에 25건이 진행되고 있는 등 많은 첨단바이오의약품이 임상 중후반 단계에 진입했습니다.
재생의료산업 전망
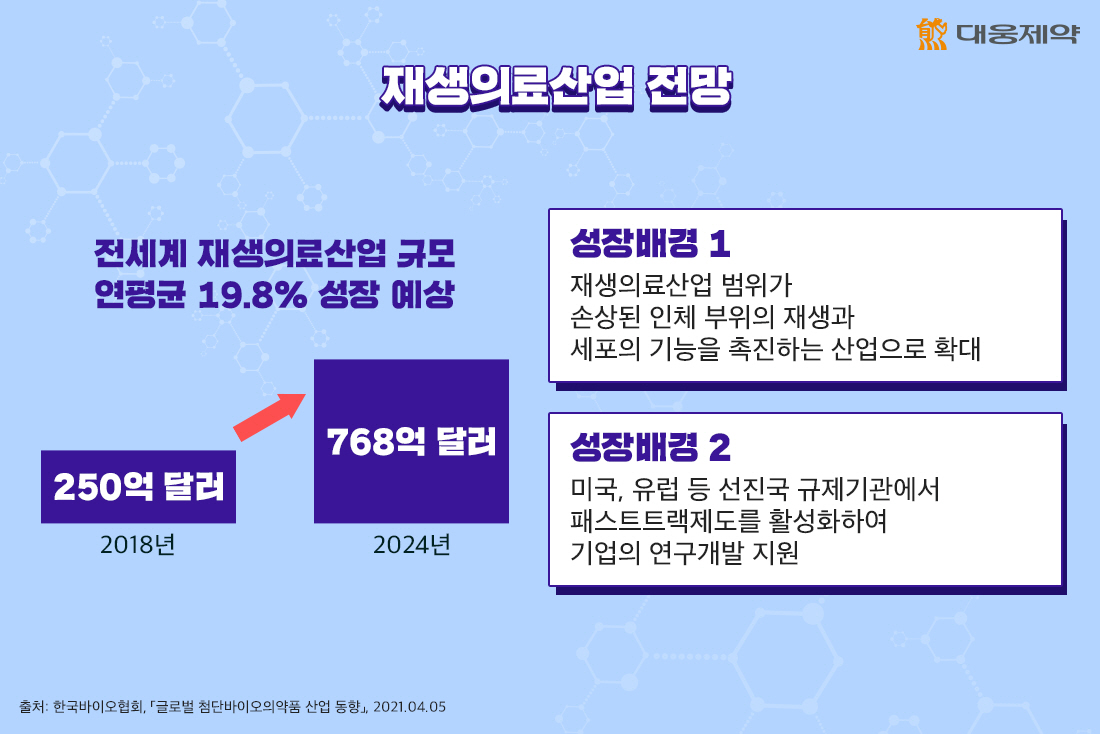
앞으로도 재생의료산업은 성장을 거듭할 것으로 보이는데요. 해외 시장조사 기관에서도 전세계 재생의료산업 규모를 2018년 250억 달러(약 28조 475억 원)에서 2024년까지 768억 달러(86조 1,619억) 규모로 연평균 19.8% 성장할 것으로 전망하고 있습니다.
이러한 성장의 배경에는 재생의료산업의 방향이 체세포, 줄기세포기반 산업에서 면역세포치료제, 유전자치료제 산업 중심으로 변화되고 있기 때문으로 볼 수 있는데요. 다시 말해 재생의료산업의 범위가 손상된 인체세포와 조직, 장기를 대체하거나 재생시켜 정상적으로 기능하게 만드는 의료 산업의 범위에서 손상된 인체 부위의 재생과 세포의 기능을 촉진하는 산업으로 개념이 넓혀지고 있다고 할 수 있습니다.
또한, 미국, 유럽 등 선진국 규제기관에서는 첨단바이오의약품의 신속한 인허가 절차를 지원하는 패스트트랙제도를 활성화하여 기업의 연구개발을 지원하고 있는데요. 미국 식품의약국(FDA)의 RMAT(Regenerative Medicine Advanced Therapy)이나 유럽 의약품청(EMA)의 PRIME(Priority Medicines)과 같은 첨단재생의료치료제 패스트트랙 제도가 파이프라인 개발을 촉진하고 있습니다. 이러한 정책에 힘입어 미국 식품의약국(FDA)과 유럽 의약품청(EMA)은 오는 2025년까지 각 기관별로 연간 10~20건의 세포 및 유전자 치료제를 승인할 것으로 예상되고 있습니다.
이러한 흐름에 맞춰 첨단바이오의약품의 개발과 생산을 지원하기 위한 위탁개발생산기업(CDMO)들도 대폭 투자를 확대하고 있는 상황입니다.
국내 제약·바이오 업계의 대응 방안

지금까지 살펴 본 글로벌 동향을 반영하여 국내에서도 재생의료산업의 임상개발 및 심사의 신속한 절차를 진행할 수 있도록 패스트트랙 제도를 활성화하여 국내 기업들의 연구개발을 촉진할 수 있도록 지원이 필요하겠습니다. 또한, 첨단바이오의약품의 국내외 연구개발 및 생산 수요에 대응하고 해외기업들과 경쟁할 수 있는 국내 CDMO의 역량 강화도 요구됩니다.
아울러, 국내 재생의료산업은 다수의 특허를 출원함으로써 그간 양적 성장을 해왔지만, 상대적으로 해외출원비율이 낮고 특허 영향력이 적어 글로벌 시장에서 경쟁력이 낮은 편으로 분석되고 있는데요. 이에, 국내 첨단바이오의약품 산업 경쟁력 확보와 글로벌 진출을 위해서는 질적으로 우수한 연구개발 성과를 선별하여 글로벌 지식재산권을 확보하기 위한 전략이 요구되는 상황입니다.
지금까지 살펴본 바와 같이 글로벌 재생의료산업은 난치성 질환의 치료 대안으로 떠오르며 향후 지속적인 성장을 거듭할 것으로 예상되는데요. 우리나라 제약·바이오 기업들도 재생의료산업의 글로벌 경쟁력을 갖춰 첨단바이오의약품 개발에 성과를 거둘 수 있기를 응원합니다.
※ 출처: 한국바이오협회, 「글로벌 첨단바이오의약품 산업 동향」, 2021.04.05
1) 생명공학정책연구센터, BioINpro 2016년 전문가 리포트 21호 ‘재생의료 동향 및 전망’, p.1




